
基于RuCo双金属纳米片的类酶活性用于炎症性肠病治疗

炎症性肠病(IBD)是一种常见的慢性炎症性疾病,具有难治愈、高复发的临床特征,严重影响患者生活质量。目前临床主要治疗方案包括水杨酸制剂、糖皮质激素和免疫抑制剂(如英夫利昔单抗、维多珠单抗等),但这些药物存在疗效有限、易产生耐药性及免疫抑制相关感染风险等明显缺陷。研究表明,病灶部位活性氧(ROS)的过度积累是推动IBD进展的关键因素:过量ROS不仅通过激活NF-κB信号通路促进炎症反应,还会破坏肠道屏障功能,导致菌群失调。虽然基于抗氧化酶的靶向治疗理论上可行,但天然酶制剂存在制备成本高、功能单一和稳定性差等固有缺陷。近年来,模拟天然酶催化机制的纳米材料因其可设计性和稳定性优势,为开发新型抗氧化治疗方案提供了新思路。
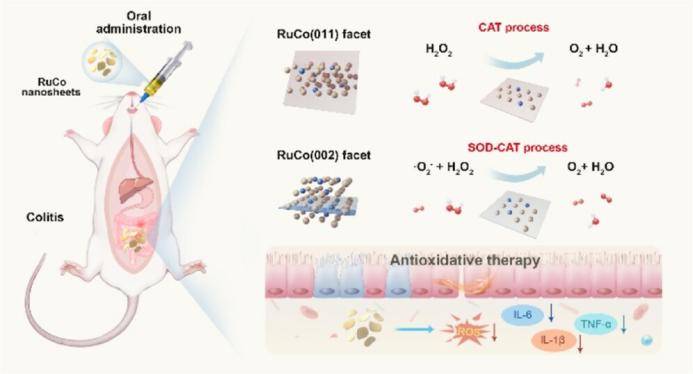
近日,中国科学院上海硅酸盐研究所的施剑林院士团队构建了一种具有合金结构的钌钴双金属纳米片(RuCo NSs),用于IBD的催化抗氧化治疗。该材料通过钌钴原子间的电负性差异优化电子结构,展现出卓越的类超氧化物歧化酶(SOD)/过氧化氢酶(CAT)级联催化活性。DFT计算结果显示,(011)晶面主要催化H2O2分解(类CAT活性),而(002)晶面则实现O2•⁻清除与H2O2转化的协同催化(类SOD-CAT活性),这种晶面特异性催化机制为精准调控抗氧化反应提供了新方法。更重要的是,钌钴双原子构型赋予材料优异的酸稳定性,使其能耐受胃肠道环境,实现口服给药治疗。体内实验证实,RuCo NSs经口服给药,能有效靶向肠道炎症部位,显著缓解氧化应激并改善病理症状,且具有良好生物安全性。该研究工作为口服给药胃肠道疾病的纳米催化治疗提供了一种新思路。
该研究工作以“A Enzyme-Mimic Activities of RuCo Bimetallic Nanosheets for Inflammatory Bowel Disease Treatment”为题发表在Journal of the American Chemical Society上(2025, DOI: 10.1021/jacs.5c00100)。第一作者为2019级直博生陈志鑫(已毕业),通讯作者为施剑林院士和林翰副研究员。研究工作得到了国家重点研发计划、国家自然科学基金、中国科学院青年创新促进会项目、CAST青年精英科学家赞助计划项目、上海市科学技术委员会新星计划项目、CAMS医学科学创新基金项目的资助和支持。
论文链接:https://pubs.acs.org/doi/10.1021/jacs.5c00100

