一、用于复杂组织再生修复与组织工程的新型无机生物活性材料
生物材料在再生医学中主要以植入材料的形式发挥重要作用,其释放的离子化学信号可诱导细胞生长、增殖和分化,从而调控复杂组织再生修复。如何构建调控仿生离子微环境、并创制提供仿生离子微环境的高纯度生物陶瓷原材料,是促进复杂组织再生修复的关键。
课题组通过采用固相法、化学沉淀法、水热法、溶胶凝胶法、无容器悬浮技术等多种方法,设计并实现对各种生物材料的化学组成的调控,构建了多种仿生组成生物玻璃、生物陶瓷的“生物材料库”。例如包括Si-Ca体系的硅酸钙(CaSiO3)、硅酸二钙(Ca2SiO4)和硅酸三钙(Ca3SiO5)、Si-Mg体系的硅酸镁(MgSiO3)与硅酸二镁(Mg2SiO4)、Si-Zn体系的硅酸锌(Zn2SiO4)、Si-Sr体系的硅酸锶(SrSiO3)、Si-Ca-Mg体系的镁黄长石 (Ca2MgSi2O7)与白硅钙石(Ca7MgSi4O16)、Si-Ca-Zn体系的锌黄长石(Ca2ZnSi2O7)、Si-Ca-P体系的叠磷硅钙石(Ca7Si2P2O16)、Si-Ca-Li体系的硅酸钙锂(Li2Ca2Si2O7和Li2Ca4Si4O13)等。在此基础上,对硅酸盐生物活性陶瓷的活性机理进行了深入研究,发现硅酸盐陶瓷在降解过程中释放硅离子(Si)等生物活性离子显著地促进骨组织细胞的增殖、分化及骨组织修复(图1);揭示Si离子促进成骨的机制在于激活AMPK/ERK1/2和PI3K/Akt及Wnt相关的信号通路,并阐明Si离子与其他微量离子的组合与协同效应和Si离子对细胞间的相互作用及其旁分泌机制(图2),推动生物陶瓷从传统磷酸钙体系拓展到具有“主动成骨”功能的钙硅基体系。
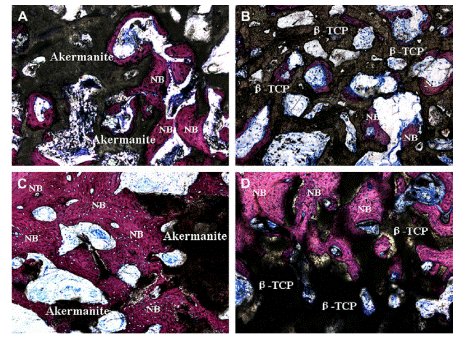
图1.多孔镁黄长石(A、C)、β-TCP(B、D)生物陶瓷支架植入兔子股骨8w(A、B)、16w(C、D)后骨组织与材料界面间的组织学观察结果
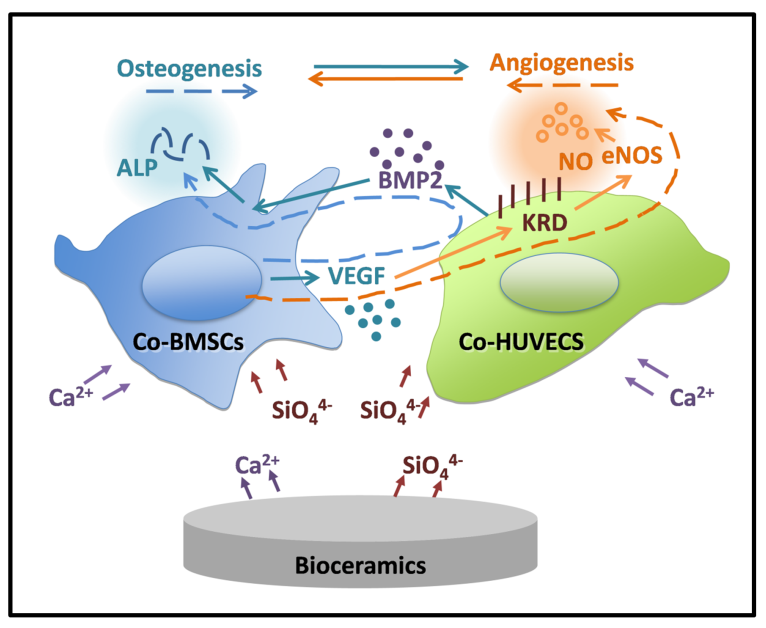
图2.硅酸钙释放的生物活性离子可以调控骨髓间充质干细胞和内皮细胞的相互作用从而促进成骨和成血管
在此基础上,课题组成功制备了含锂、铜、钼等活性离子的硅酸盐陶瓷支架,发现该类材料不仅能够促进关节软骨下骨的修复,同时还能够促进关节软骨缺损的愈合与再生,充分体现了该类材料修复骨-软骨的双向功能特性(如图3所示,Biomaterials 2019,196:138-150,Advanced Science 2023, 10(13): 2206875(1-14));此外,发现含锂硅酸盐陶瓷材料不仅能够用于骨-软骨修复,同时还能够显著地诱导牙周膜干细胞的成骨成牙分化,其机制与激活Wnt/β-catenin和ERK信号通路密切相关,有望用于牙周缺损修复与再生(Applied Materials Today, 2019, 16: 375–387)。
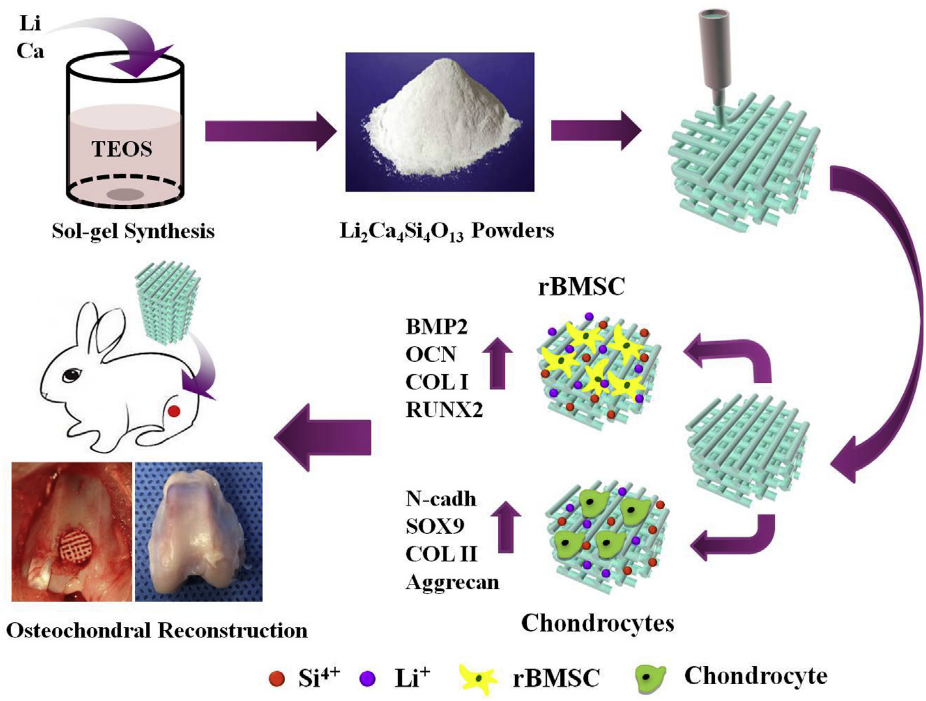
图3. 硅酸盐生物陶瓷支架在骨软骨重建中的应用示意图
在软组织修复方面,课题组研究发现锶(Sr)离子对多种心血管细胞均有激活作用,如促进内皮细胞、平滑肌细胞和成纤维细胞的增殖、迁移、分泌血管生成相关因子及细胞间相互作用;抑制心肌细胞凋亡,抵抗低氧无糖损伤。继而设计和制备了具有可注射性、可降解性、可缓释合适浓度锶离子的复合水凝胶。在小鼠心肌缺血/再灌注(60分钟/20分钟)后注射锶离子复合水凝胶,可以显著改善心肌缺血/再灌注小鼠心功能、减小疤痕面积。这些心肌修复作用伴随着血管数量增加和血管生成相关因子表达升高、凋亡心肌细胞数量减少、凋亡相关蛋白酶活性以及血清乳酸脱氢酶活性降低。本研究揭示了缓释活性锶离子的可降解水凝胶可通过改善心肌缺血/再灌注后心肌细胞存活、促进血管新生有效恢复损伤心脏心功能和抑制纤维疤痕,它可能以较低的成本,更高的稳定性和潜在的更高的安全性为缺血性心脏病提供一种新的治疗方法(如图4所示,Science Advances, 2021, 7: eabe0726)。
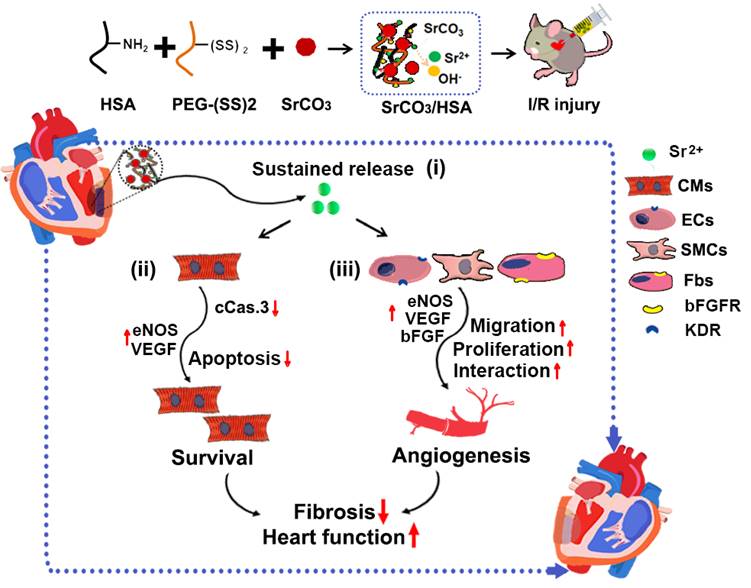
图4.锶离子复合水凝胶对心肌缺血/再灌注损伤的修复作用模式
此外,基于钼元素的免疫调节作用,课题组开发了一种基于钼酸钙(CM)纳米颗粒的生物墨水,并引入真皮毛乳头细胞(DPCs)和巨噬细胞构建出具有免疫调节功能的多细胞支架(如图5所示,Nano Today 2023, 51: 101917)。支架通过释放Mo离子诱导巨噬细胞极化为M2表型,形成抗炎免疫微环境进一步刺激了真皮毛乳头细胞中毛囊生长期相关细胞因子的分泌。通过裸鼠创面、皮下植入和小鼠的雄激素脱发三种动物模型证实了该支架的免疫调节和诱导毛发再生作用。
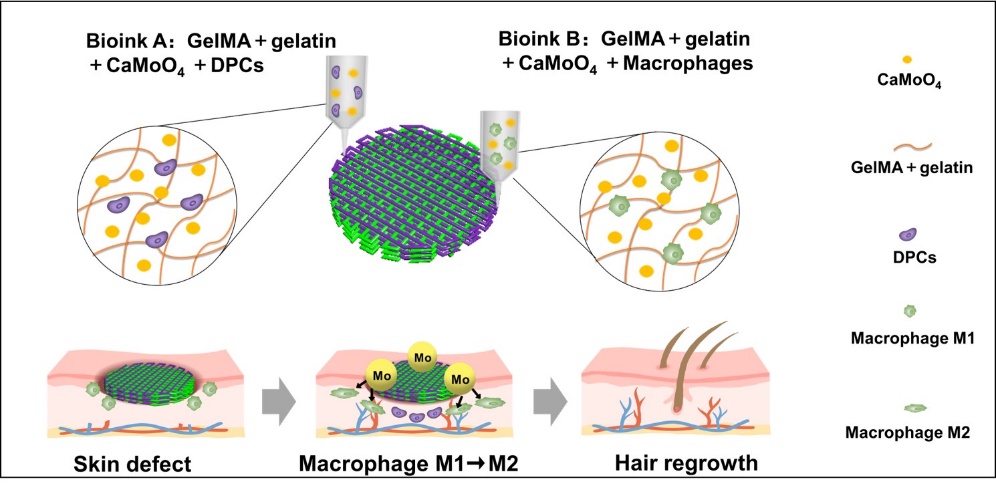
图5.基于含钼酸钙的生物墨水,利用具有免疫调节功能的多细胞支架促进毛发再生
越来越多的研究表明具有特定化学组成和形貌结构的生物陶瓷具有调节干细胞的命运以及与其微环境相互作用的活性,从而增强了包括硬组织和软组织在内的组织再生(如图6所示,Materials Today 2019,24,41-56)。
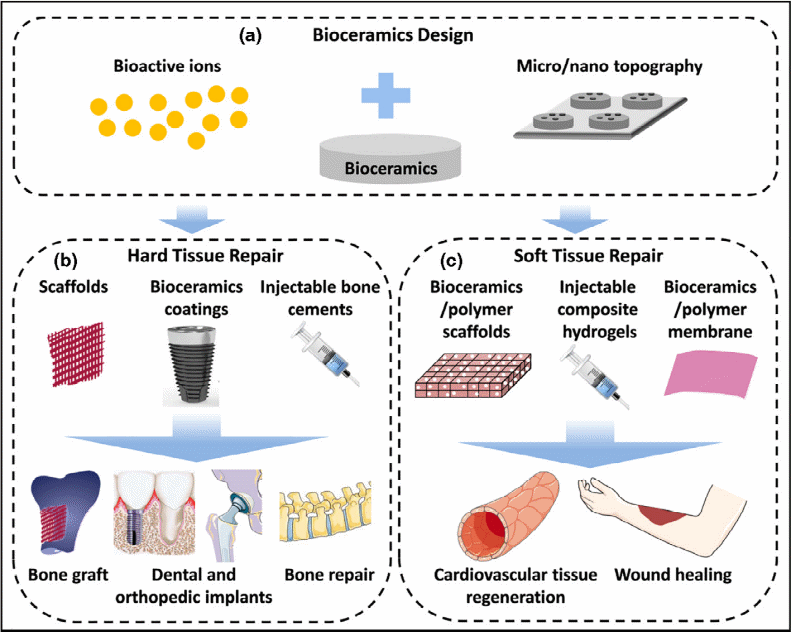
图6. 生物陶瓷用于组织再生修复的设计原理和潜在应用领域。(a)生物陶瓷材料的设计:生物陶瓷的化学组成和微/纳米表面形貌是材料设计中要考虑的两个关键因素;(b)多孔形式的生物陶瓷支架、可注射的骨水泥或金属或聚合物的复合材料可用于硬组织再生;(c)生物陶瓷与生物聚合物可以设计成多孔复合支架、可注射复合水凝胶和电纺丝纤维膜的形式用于创口修复和心血管组织再生等应用。
二、生物材料数字化智能制造与生物3D打印用于组织/器官再生再造
1. 3D打印仿生结构生物陶瓷支架
骨的复杂多级结构赋予其优异生物学和力学性能,但也增加骨组织修复难度。如何仿生设计生物材料高效促进骨组织复杂结构与功能完整修复再生,对生物材料发展至关重要。受到自然界骨、莲藕等天然材料多级结构与功能之间关系的启发,课题组率先提出将仿生理念与3D打印技术结合,发展系列3D打印仿生结构生物陶瓷支架用于血管化骨再生。
基于莲藕内部多通道结构的启发,采用3D打印制备出仿生莲藕生物陶瓷支架。仿生多通道结构赋予了材料更高的比表面积,加速了生物活性离子的释放,进而诱导间充质干细胞成骨相关基因(Runx2、ALP、OCN)高表达,并可抑制内皮细胞ARPIN蛋白表达,增强肌动蛋白聚合调节因子ARP 2/3蛋白表达,从而促进内皮细胞迁移,体内实验结果也进一步证明该仿生材料通过释放生物活性离子与莲藕孔道结构协同加速血管化骨再生,相比于实心陶瓷支架,多通道陶瓷支架组新骨形成面积提高3.5倍(如图7所示,Advanced Science2017, 4: 1700401;Biomaterials2017, 135: 85-95)。受到热狗结构启发,进一步结合双定向冰模板法与3D打印技术,在支架宏观中空通道内构筑有序多层棒状结构,发现这种中空管道及其内部有序层状结构可高效实现骨组织再生修复(Advanced Science 2019, 6: 1901146)。受树木多级结构的启发,课题组通过光固化3D打印技术实现了生物陶瓷支架树状结构构筑,并证实交叉状树状结构显著提高细胞增殖效率,特别是其多级结构特征可用于递送骨驻留细胞和神经驻留细胞并诱导成骨及成神经 分化,实现神经化骨组织再生(Additive Manufacturing 2022, 54:102721)。
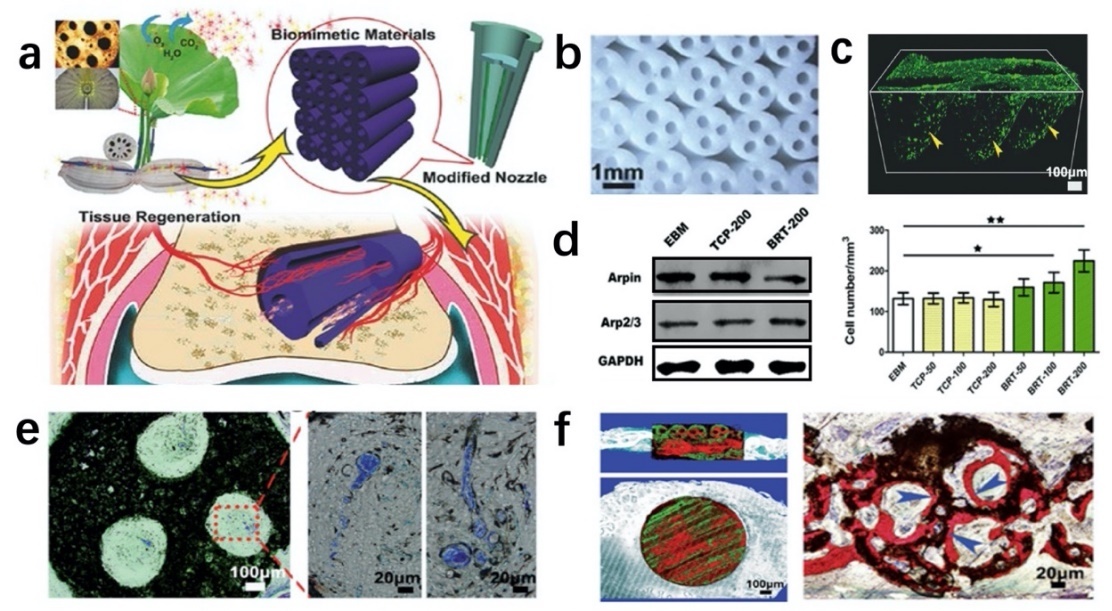
图7. 受自然界启发制备出仿生莲藕支架用于骨组织工程(a),支架仿生莲藕多通道结构(b)促进细胞黏附(c),增强内皮细胞迁移相关蛋白与骨髓干细胞成骨分化基因表达(d),从而促进体内血管化骨再生修复(e,f)。
为更好地实现骨组织完整结构与功能修复,课题组通过仿生天然骨多级结构,实现骨哈弗斯管、福尔克曼管及松质骨多结构一体化打印及精细调控,并模拟骨的多细胞组成与空间分布,基于仿生结构单元实现多细胞(骨髓间充质干细胞、内皮细胞、雪旺细胞等)协同负载递送,以此促进骨髓间充质干细胞ALP表达和一氧化氮产生,进而通过旁分泌效应激活内皮细胞血管生成基因标志物激酶结构域受体、一氧化氮合成酶和钙粘蛋白的表达,从而启动成骨分化及成血管分化,促进血管化骨组织再生,其新骨生成面积提高1倍、新生血管面积提高3倍(如图8所示,Science Advances2020, 6: eaaz6725)。
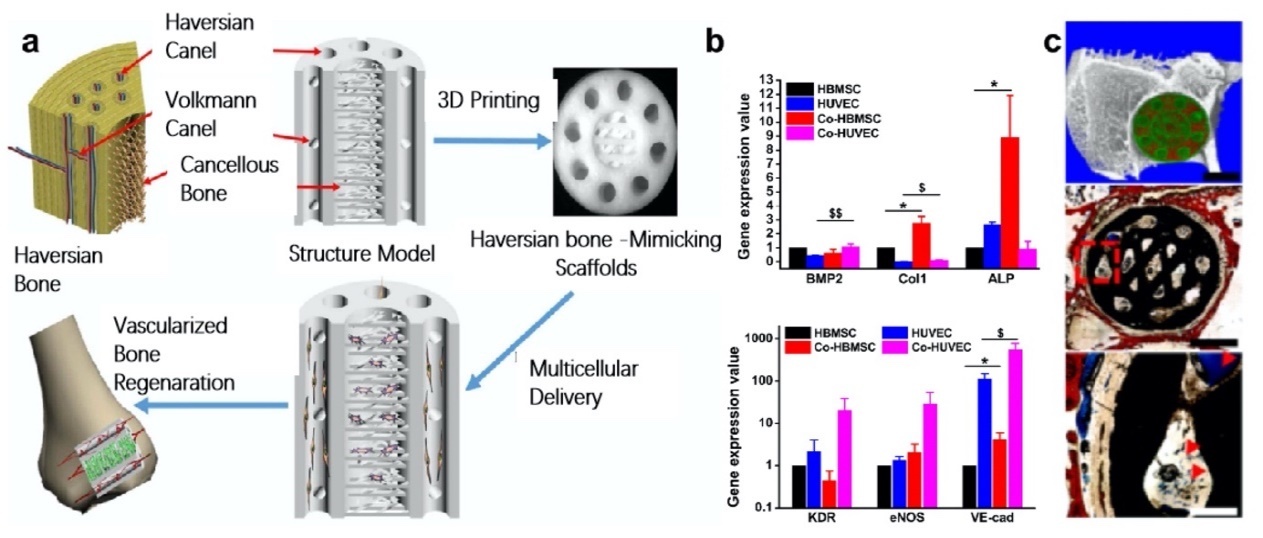
图8. 3D打印仿哈弗斯骨生物陶瓷支架构建的多细胞递送系统(a),仿哈弗斯结构通过激活多种细胞间相互作用、增强内皮细胞成血管分化与间充质干细胞成骨分化(b),进而显著加速体内血管化再生(c,红色箭头指示为新生血管)
基于生物陶瓷仿生孔道结构可高效提升其骨修复能力的研究基础,课题组进 一步探究了三维多孔支架的仿生微纳米表面结构对材料成骨性能的影响。受自然 界中微生物矿化现象的启发,课题组采用微生物辅助催化方法,在多孔生物陶瓷 支架表面成功构建了形貌可控的仿生碳酸钙矿物微纳米结构,发现这种独特的仿 生矿物结构更有利于促进骨髓间充质干细胞的粘附、铺展和成骨基因表达,并通过调控干细胞Wnt信号通路,显著上调介导细胞粘附的Itga2等基因表达,更有 利于促进骨髓间充质干细胞的粘附、铺展和后续的成骨分化。体内研究结果表明, 微生物矿化形成的表面微纳结构能够抑制硅酸钙陶瓷支架快速降解,并且显著促 进新骨的形成,从而快速的实现骨组织修复与再生(如图9所示,Advanced Materials,2021, 2104829)。
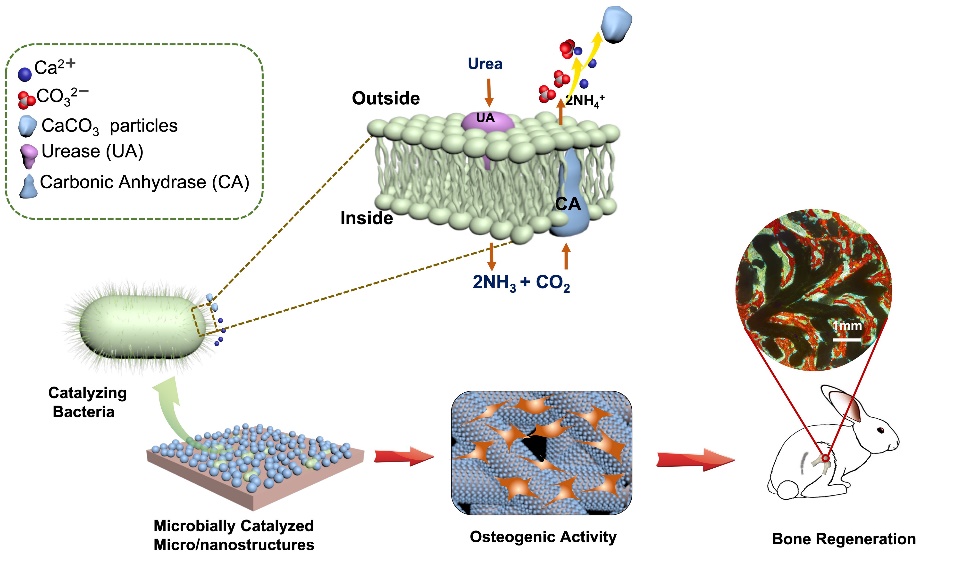
图9.利用微生物矿化作用制备微/纳米结构及其在骨再生中的应用
骨骼不仅具有复杂精密的多级结构,密集的神经和血管网络还并行穿过皮质骨中的哈弗斯管和福尔克曼管进入到骨髓腔中调控骨骼的稳态。课题组使用光固化3D打印技术成功制备了一系列具有不同三维拓扑结构的空间填充多面体生物陶瓷支架来有效模拟松质骨的不规则多孔网状结构。研究发现,空间填充多面体生物陶瓷支架的力学强度和孔隙率可以通过程序化设计进行灵活调控,以满足不同患者的个性化需求。计算流体动力学(CFD)模拟分析结果表明空间填充多面体支架相比于传统交叉堆叠结构支架具有相对较低的平均壁面压力,有助于细胞的驻留及黏附。空间填充多面体生物陶瓷支架不仅可以激活PI3K-Akt信号通路促进骨髓间充质干细胞的增殖和成骨分化相关基因的表达,还可以显著促进内皮细胞成血管相关蛋白的表达以及神经元的轴突延伸,表现出优异的神经和血管调控能力。体内动物实验结果进一步表明空间填充多面体支架可以更好的促进新生骨的形成、诱导血管化及神经纤维的长入,进而实现了高效的神经/血管化骨再生(如图10-11所示,Advanced Materials 2023, 35:2302716)。
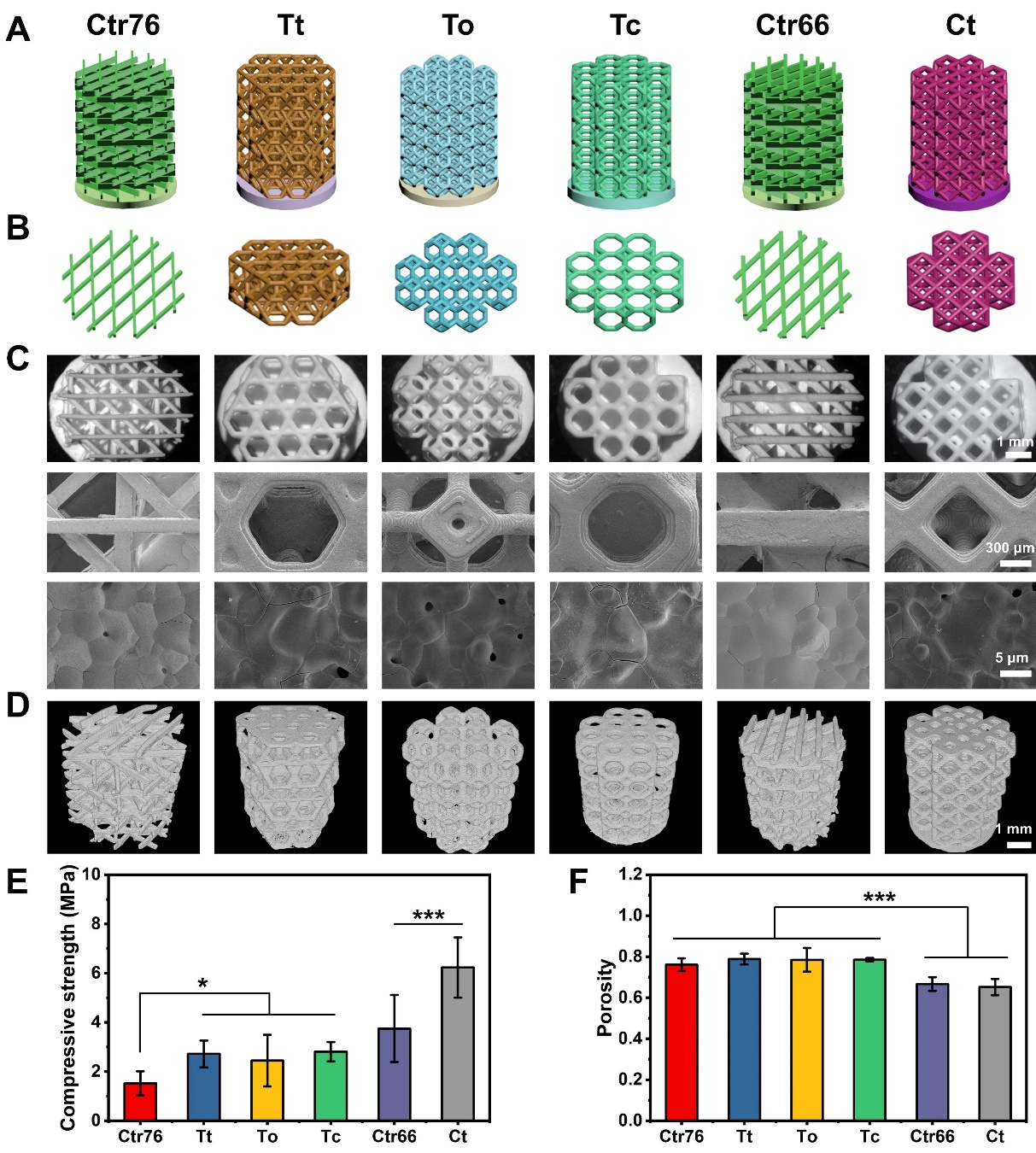
图10. 3D打印空间填充多面体生物陶瓷支架的制备与表征。(A-B)不同空间填充多面体支架的设计模型图;(C)不同空间填充多面体支架的实物图及扫描电镜图片;(D)不同空间填充多面体支架的Micro-CT重建图像;(E)不同空间填充多面体支架的力学强度;(F)不同空间填充多面体支架的孔隙率。
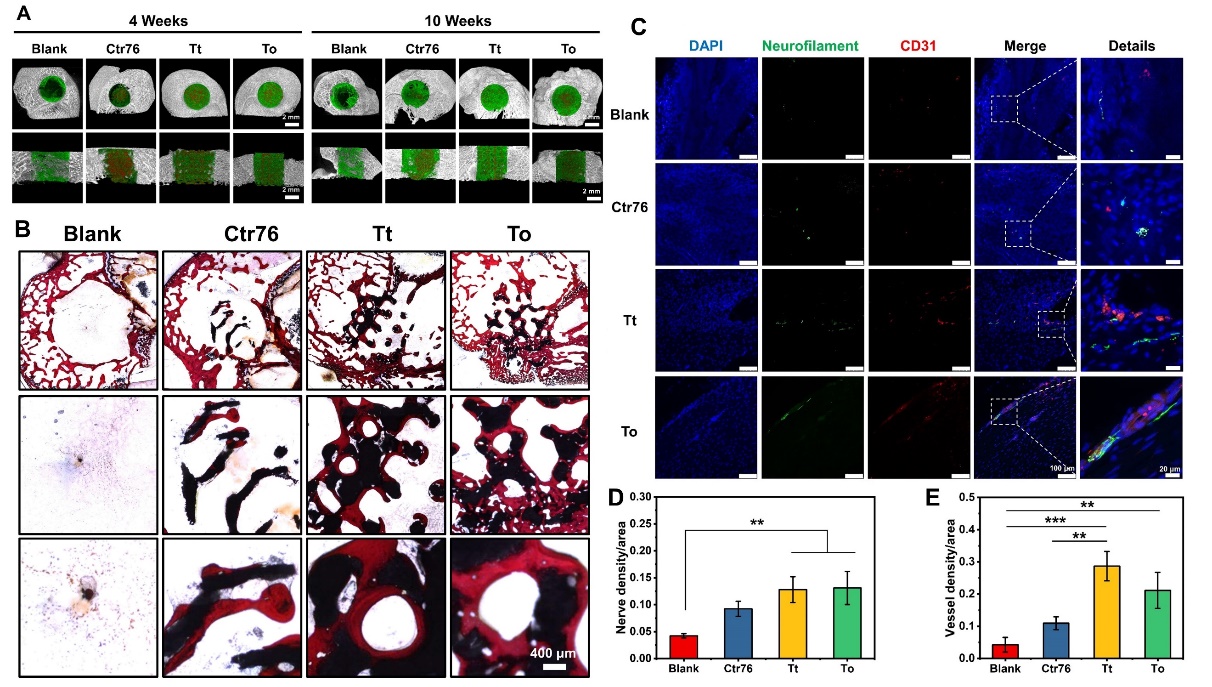
图11. 3D打印空间填充多面体生物陶瓷支架促进体内神经/血管化骨再生。(A)支架在植入骨缺损处4周和10周时的Micro-CT重建图像;(B)骨缺损处的硬组织切片染色;(C)骨缺损处的神经和血管双重免疫荧光染色;(D-E)骨缺损处的神经和血管统计学分析。
组织驻留细胞的行为可能受到细胞相互作用的空间排列的影响。因此,精确控制多细胞构建体中各种细胞的空间组织具有重要意义。然而,构建一种具有多种细胞类型有序空间组织的多功能多细胞支架仍然具有挑战性。课题组通过组装各类载有细胞的模块,构建了具有不同细胞类型有序空间分布的模块化多细胞组织工程支架。有趣的是,模块化支架可以分解成单独的模块,以评估系统中每种细胞类型的具体贡献。通过组装载细胞模块,研究成功建立了巨噬细胞-间充质干细胞(MSC)、内皮细胞-MSC和软骨细胞-MSC共培养模型。体外实验结果表明,细胞间串扰可以促进系统中各种细胞类型的增殖和分化。此外,模块化支架中的MSCs可通过活化T细胞核因子(NFAT)信号通路调节软骨细胞的行为。此外,与其他组相比,负载共培养软骨细胞MSC的模块化支架表现出增强的骨软骨组织再生能力。该研究工作为构建多细胞组织工程支架提供了一种很有前途的策略,用于细胞间串扰和复杂组织工程的系统研究(如图12所示,Advanced Materials2024, 2308126)。
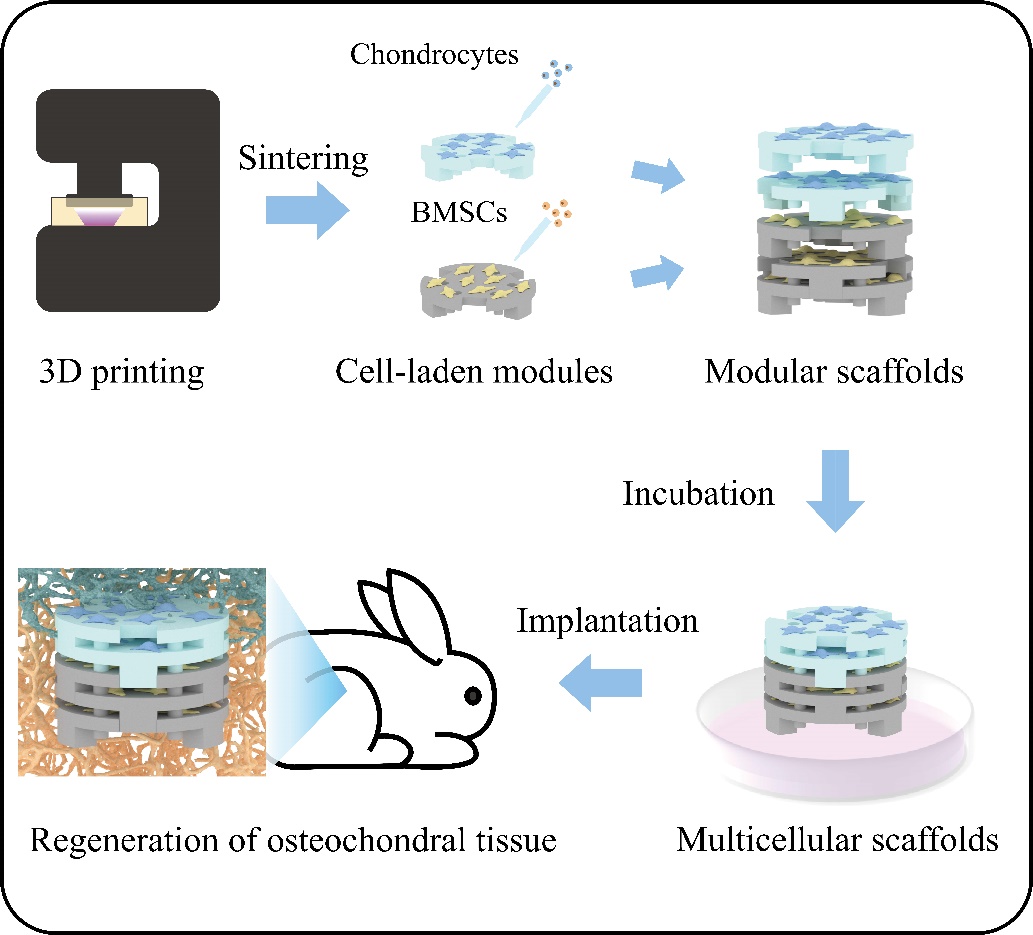
图12. 模块化多细胞组织工程支架在骨软骨重建中的应用示意图
- 仿生多细胞3D打印支架
细胞3D打印是一种先进的生物制造技术,利用该技术可以轻松实现多种材料、多种细胞和生物活性因子的精确定位与分布,为复杂组织和器官再造奠定基础。课题组在骨软骨、肌腱骨、神经骨、皮肤修复再生等方面进行了一系列探索研究。
2.1 骨软骨修复
关节软骨和软骨下骨各向异性的生理特性和双向分化的需求使骨-软骨组织的仿生重建面临巨大的挑战。根据软骨和软骨下骨中不同的细胞类型和生理需求,课题组首先开发了基于Li-Mg-Si(LMS)生物活性陶瓷的生物墨水,并利用细胞生物3D打印技术,通过控制生物墨水及细胞的组成和分布,构建了含有软骨细胞和间充质干细胞的多细胞体系,以模拟骨-软骨组织各向异性的生理环境。生物打印的多细胞支架被设计为两层,其中软骨层为负载软骨细胞的水凝胶生物墨水,软骨下骨层是负载有间充质干细胞的含LMS生物陶瓷的生物墨水。细胞和生物墨水的这种组成和空间设计能够满足软骨和软骨下骨中不同细胞增殖和分化的需求。生物3D打印的多细胞支架显示出优异的细胞活力,空间分布和递送效率,其在体外能够调节多种细胞的分化行为,并在体内有效促进了大块骨-软骨缺损的修复(如图13所示,Materials Today2021,49:68-84)。
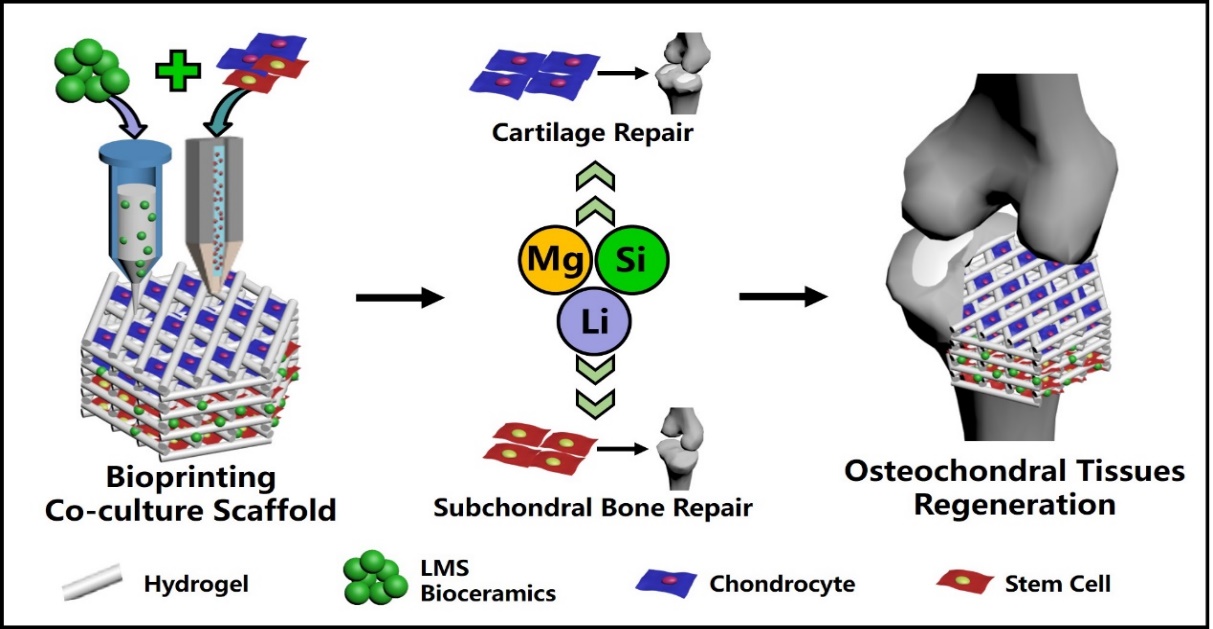
图13.将含有LMS生物陶瓷的生物墨水与多细胞相结合,通过3D生物打印方法制备模拟骨-软骨组织的双层多细胞支架修复骨-软骨缺损
2.2肌腱骨修复
肌腱-骨界面独特的分层结构和梯度成分可有效缓解应力集中,在人体运动功能中发挥着重要作用。课题组通过将肌腱/骨相关细胞(肌腱干细胞TSPCs/骨髓间充质干细胞BMSCs)与含钼的硅酸盐(MS)生物陶瓷相结合,开发了一种模拟肌腱/骨组织的生物仿生墨水。随后通过3D生物打印技术制造了生物仿生多细胞支架,通过生物仿生墨水的空间分布实现了对肌腱与骨界面的分层结构和细胞组成的模拟,这对于诱导界面区域复杂结构的再生具有重要意义。得于MS生物陶瓷创造了理想的离子微环境,生物仿生支架在体外表现出同时诱导 TSPCs 成肌腱分化和 BMSCs 成骨分化的双向分化能力。同时证明了Mo离子对于双向分化的重要作用,并发现Mo离子主要通过TGFβ通路促进TSPCs成肌腱分化。兔子的肩袖损伤模型中,仿生多细胞支架展现出促进骨修复、肌腱成熟、纤维软骨形成、胶原沉积和生物力学改善方面表现出最佳能力,在体内实现了令人满意的肌腱-骨界面再生。该研究为构建具有双重功能的生物仿生多细胞支架以诱导多谱系组织再生,尤其是软硬组织界面再生提供了可行的策略(如图14所示,Advanced Science 2023, 10(21): 2301309)。
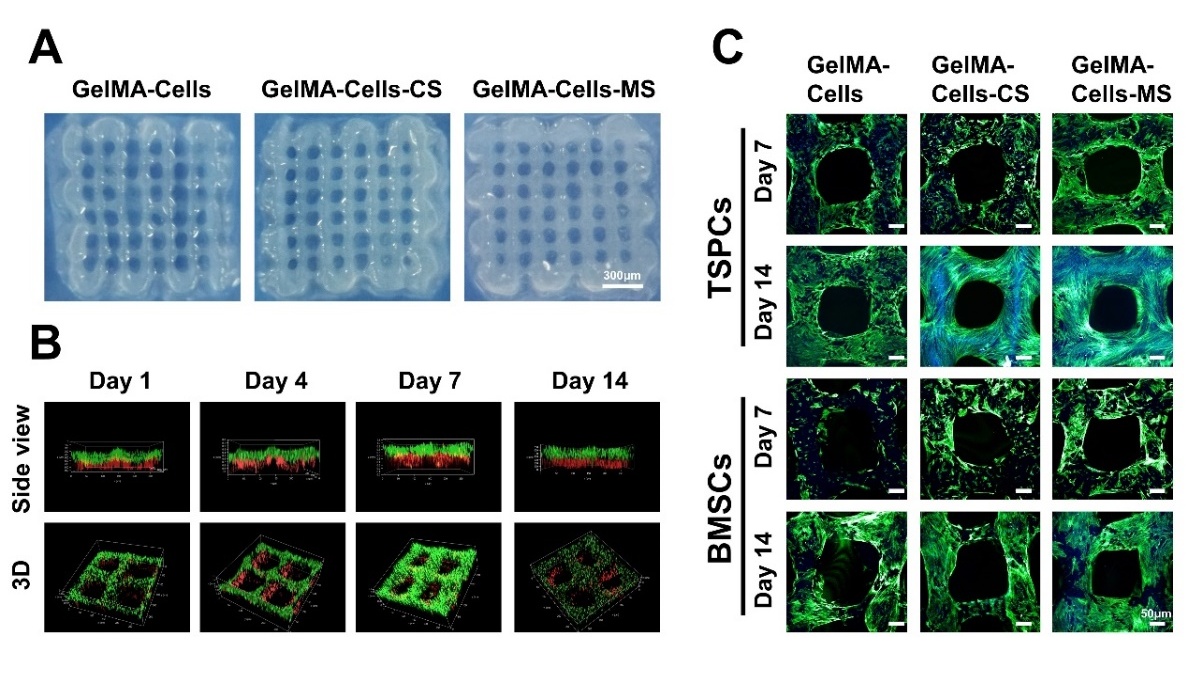
图14.构建具有肌腱-骨结构和组成特点的仿生多细胞支架
在此研究基础上,课题组进一步通过多细胞打印技术将硅酸锰(MS)纳米颗粒与肌腱/骨相关细胞相结合,设计并构建了具有免疫调控功能的多细胞支架,用于肌腱和骨的一体化再生(如图15所示,Science Advances 2024,10:adk6610)。该免疫调节支架不仅在体外展现出多样性的生物活性,而且在多种肩袖损伤(RCT)动物模型中实现了免疫调节、多组织一体化再生和运动功能恢复。通过对其免疫生物学机制的探索,免疫多细胞支架能够稳定释放Mn离子刺激巨噬细胞分泌 PGE2,从而增强多细胞的特异性分化。总之,免疫多细胞支架的构建为软硬组织界面的一体化再生提供了一种前景广阔的新策略。
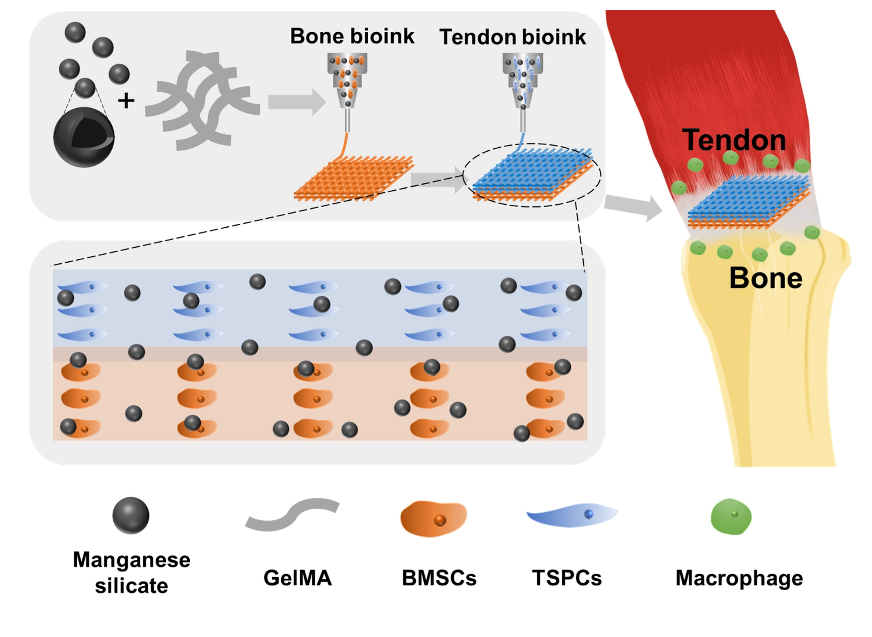
图15. 基于硅酸锰(MS)纳米颗粒的免疫多细胞支架用于肌腱-骨一体化再生的示意图
自然界是一个多物种共存的生态系统,其中,跨物种共生是一种典型的生物学现象。受到海洋藻类为各类生物和周围环境提供充足氧气及营养物质的启发,课题组研究团队提出通过跨物种共生实现海洋硅藻活体驯化哺乳动物细胞的理念,将硅藻与哺乳动物组织细胞结合,采用3D生物打印技术,设计了一种硅藻活体衍生的跨物种构建体,改善肌腱细胞微环境,促进肌腱-骨界面损伤修复(如图16所示, Materials Today https://doi.org/10.1016/j.mattod.2024.12.010)。跨物种支架具有独特的优势,自发荧光便于观察,自主光合可持续供氧,硅藻可降解的硅质细胞壁利于硅离子释放,通过MAPK/cAMP/昼夜节律信号通路激发肌腱干/祖细胞的成肌腱分化,为促进肌腱-骨界面组织再生提供条件。硅藻活体对大鼠皮下模型无急性不良反应和毒、副作用(图17a)。在大鼠肩袖撕裂模型中,跨物种支架在节律光照下,能够缓解损伤部位乏氧,促进大鼠运动功能恢复(图17b)。在兔肩袖撕裂模型中,由硅藻支架预培养分化后的肌腱支架展示出良好的肌腱-骨界面修复效果(图17c)。这种可时空控制的跨物种构建体得益于海洋硅藻固有的光合作用和硅离子释放,有望用于人体工程化组织修复与再生。
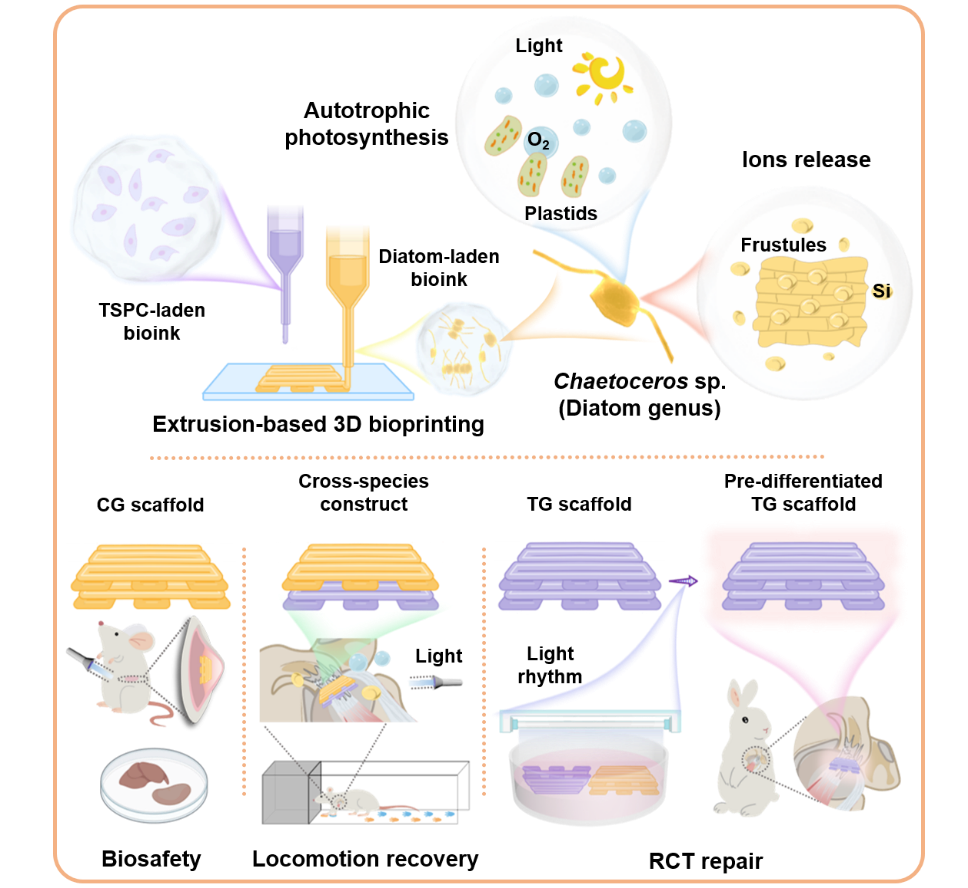
图16. 3D生物打印载角毛藻和肌腱干/祖细胞生物墨水以构建跨物种共生支架用于肩袖撕裂修复和运动功能恢复。
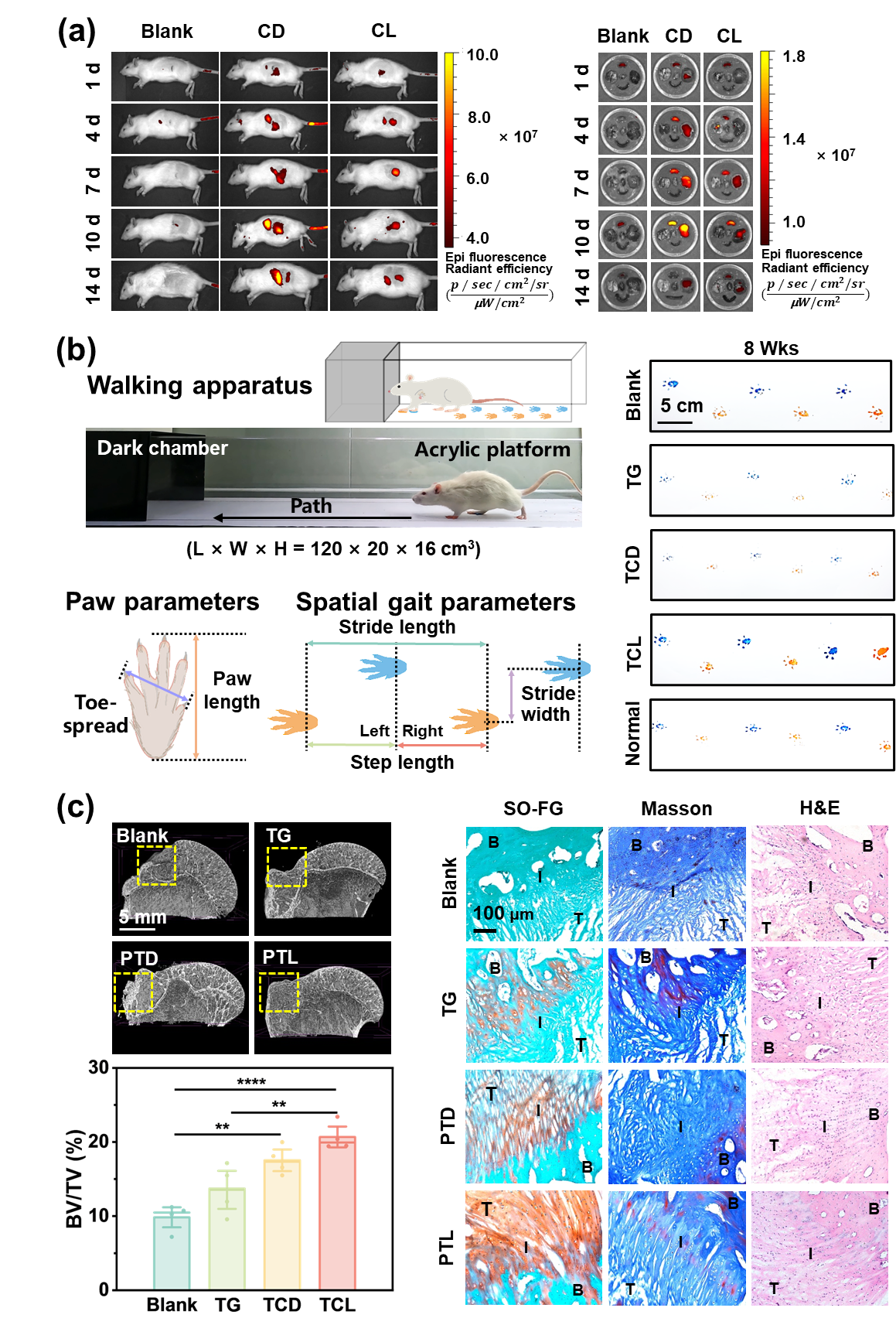
图17. 跨物种支架的体内安全性和修复效果。(a)角毛藻支架植入大鼠皮下的安全性;(b)跨物种支架缓解大鼠肩袖撕裂缺氧并促进运动功能恢复;(c)经角毛藻支架驯化后的肌腱支架促进兔肩袖撕裂修复。
2.3 神经化骨修复
骨骼是一个高度神经支配的复杂器官组织,骨内神经纤维通过分泌多种神经递质(CGRP、SP、VIP等)和神经营养因子(NGF、BDNF、GDNF等)等积极参与骨骼的生长发育与再生修复。由于骨组织与神经纤维具有显著不同的生理特性,同时实现骨和骨内神经纤维的再生目前仍旧是一个巨大的挑战。课题组提出利用无机生物墨水多细胞生物3D打印技术构建含无机硅酸钙纳米线(CS)、甲基丙烯酰化明胶水凝胶(GelMA)、骨髓间充质干细胞和神经细胞(雪旺细胞)的多细胞支架用于神经化骨的修复再生。研究发现CS可以通过缓释钙、硅离子来构建一种适宜的离子微环境来调控细胞行为,不仅可以促进雪旺细胞成熟及髓鞘化相关基因和蛋白的表达,还可以同时促进骨髓间充质干细胞成骨相关基因和蛋白的表达以及钙结节的形成。体内大鼠颅骨损伤动物实验结果表明这种基于无机生物墨水的仿生多细胞支架可以有效促进新生骨的形成、骨整合、诱导宿主神经纤维长入,从而实现了高效的神经化骨再生。本研究将功能性无机生物墨水与多细胞生物3D打印技术相结合,为实现复杂的神经化组织再生提供了一种潜在的策略(如图18所示,Nano Today 2022,46:101584)
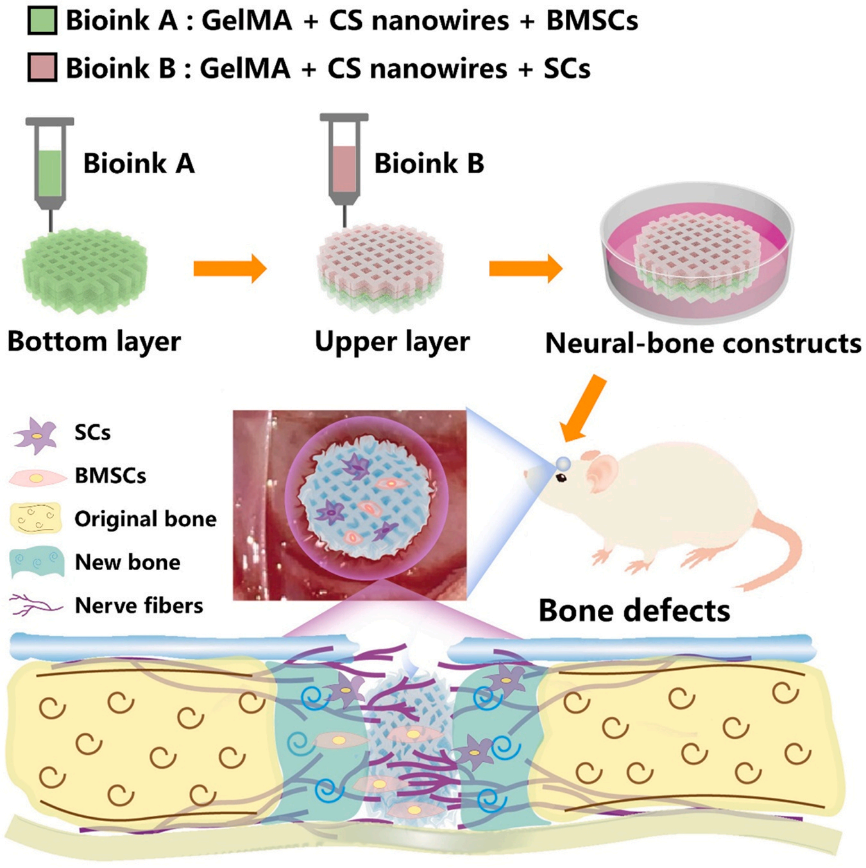
图18. 含有生物活性硅酸钙纳米线的生物墨水与雪旺细胞和骨髓间充质干细胞相结合,通过多细胞生物3D打印技术制备神经-骨复合构建体用于神经化骨再生
在此研究基础上,课题组基于锂、钙、硅元素的促神经分化及神经保护作用,开发了基于Li-Ca-Si(LCS)生物陶瓷的生物墨水,并将其与神经干细胞结合,通过生物3D打印技术制备一种功能化的神经构建体。研究发现LCS基生物墨水释放的多种活性离子能够通过PI3K-AKT通路促进神经干细胞向神经元方向分化并诱导神经元成熟,展现出优异的神经调控活性。此外,基于LCS生物墨水的神经构建体还展现出良好的多细胞调控功能,有效促进骨髓间充质干细胞的成骨分化、内皮细胞的成血管化以及与肌肉细胞形成神经肌肉接头等。在全横断脊髓损伤模型中,神经构建体能够刺激神经分化及血管化,促进脊髓损伤再生及恢复老鼠下肢运动功能;在颅骨损伤模型中,神经构建体可以有效诱导新生骨的形成、骨整合、血管化及神经支配,实现神经/血管化骨再生;在体积性肌肉损伤模型中,神经构建体能够诱导肌纤维的形成与成熟、血管化并增强神经支配,实现了神经/血管化肌肉再生。该研究从“神经调节组织再生”的角度出发制备的基于生物陶瓷/神经干细胞的神经构建体为实现复杂组织再生提供了一种潜在的策略,同时也为新一代复杂组织工程生物材料的设计提供新的思路。(如图19所示,National Science Review2024, 11 (4): nwae035)
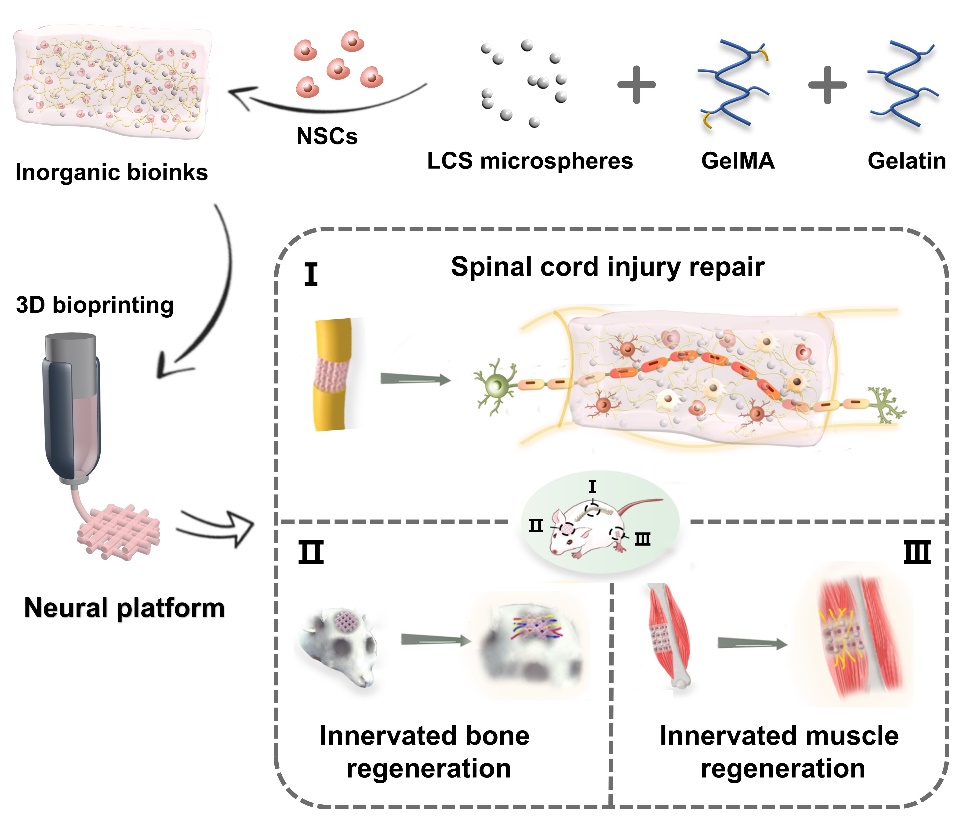
图19. 生物3D打印基于无机材料/神经干细胞的神经化构建体促进脊髓、颅骨和肌肉损伤等多种组织再生与功能恢复
2.4 皮肤修复
在血管化皮肤再生方面,课题组基于锶、硅元素对血管再生和胶原沉积的有益作用,开发了一种基于硅酸锶(SS)微米柱的生物墨水。在此基础上,打印了含有成纤维细胞和血管内皮细胞分层分布的多细胞支架,以模拟含有血管网络的皮肤的生理结构。基于SS生物墨水的优异生物活性,仿生多细胞支架能够显著促进细胞增殖和成血管化。此外,研究团队通过皮下植入、急性创面和糖尿病难愈创面三种动物模型证实了该支架可以作为皮肤替代物有效促进皮肤组织的再生(如图20所示,Advanced Healthcare Materials 2021, 10(16): 2100523)。
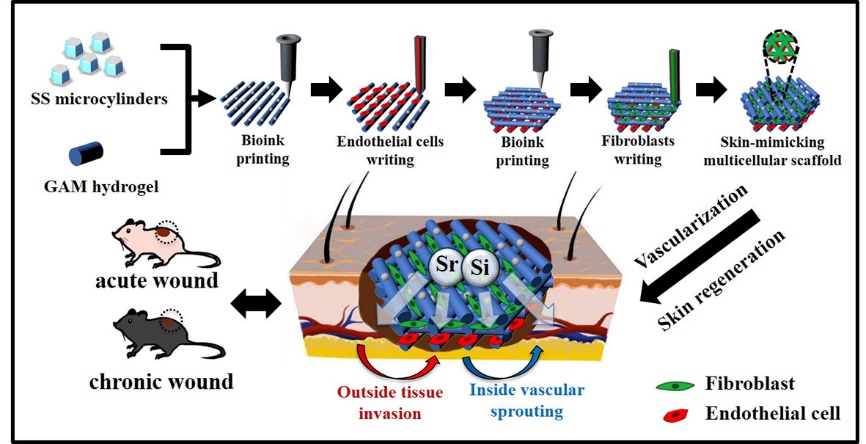
图20. 基于含硅酸锶微米柱的生物墨水,利用多细胞3D打印技术制备仿生皮肤替代物促进急/慢性创面皮肤再生
毛囊作为皮肤组织的重要附属物,在毛发生长、体温调节、分泌等方面发挥着重要作用。然而,对于成年人来说,严重损伤的皮肤及脱发导致的毛囊严重退化或受损,会导致毛发无法再生。课题组设计了一种模拟皮肤毛囊和血管结构的仿生3D多细胞微图案,并通过将硅酸镁纳米微球(MS)引入3D微图案来调控多种细胞活性,实现毛发和血管的同时再生(如图21所示,Materials Horizons2023, 10: 3773-3784)。
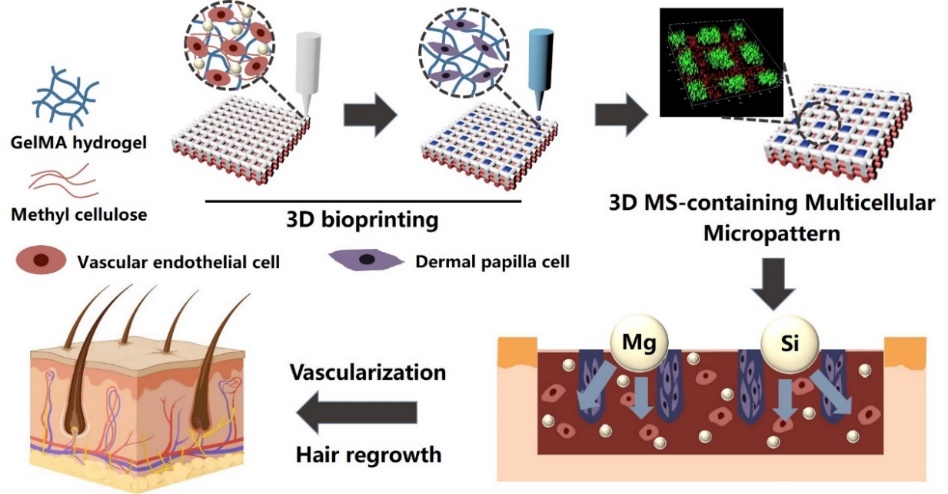
图21.生物3D打印含硅酸镁的仿生3D多细胞微图案用于毛发和血管再生
三、重大疾病治疗-组织/器官再生修复多功能生物活性材料
1. 硬组织肿瘤治疗-组织缺损修复多功能支架
肿瘤性骨缺损治疗与修复在临床上面临很大挑战,需要生物活性材料兼具肿瘤治疗与缺损修复的双功能特性。然而,目前生物材料往往只能满足单一修复要求。在系统研究生物活性陶瓷仿生结构如何主动加速促进血管化骨组织修复基础上,进一步发展兼具骨组织修复与骨肿瘤治疗双功能仿生生物陶瓷支架。课题组最早报道氧化石墨烯和聚多巴胺功能化生物陶瓷支架用于肿瘤性骨缺损治疗,实现“骨组织工程”与“骨肿瘤治疗”有机结合,开辟骨组织工程研究新方向(如图22所示,Advanced Functional Materials 2016, 26(8):1197-1208;Biomaterials2016, 111: 138-148)。
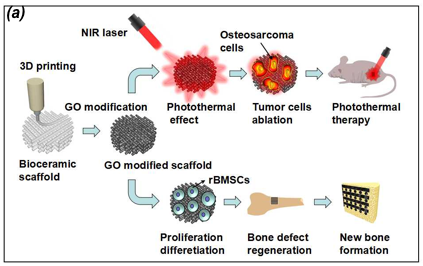
图22.氧化石墨烯修饰的生物陶瓷支架骨修复和光热抗肿瘤示意图
在此基础上,针对外源性光热试剂潜在安全性问题,通过对传统白色生物陶瓷镁热还原处理,研制形成具有本征光热特性的新一代“黑色生物活性陶瓷”。由于氧空位和结构缺陷的存在,其具有优异光热抗肿瘤功能,同时细胞生物学活性显著提升,兼具体内骨修复活性(如图23所示,Advanced Materials2020,32:2005140),为多功能生物材料设计提供了新视角。
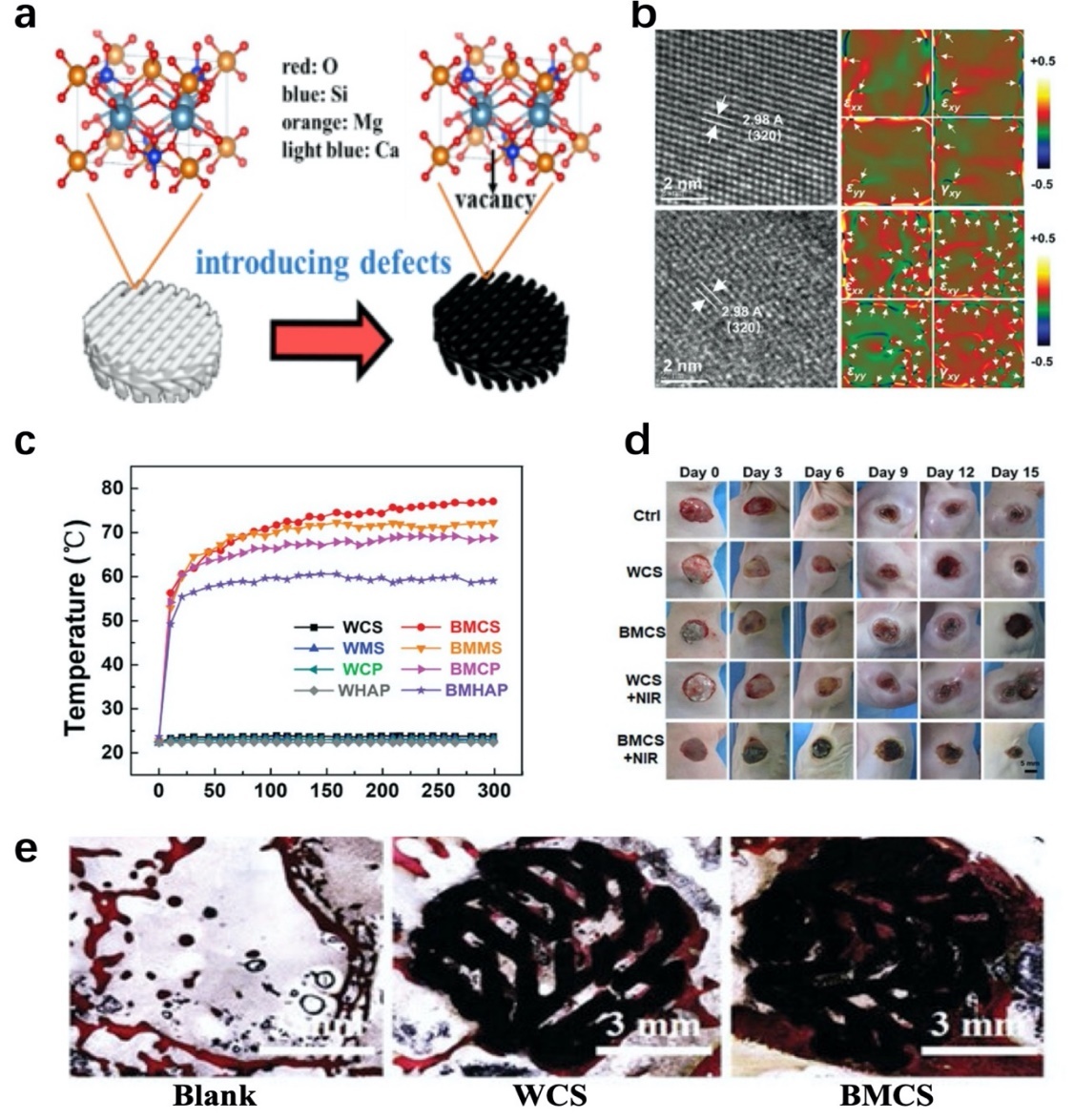
图23.黑色生物活性陶瓷(BMCS)制备策略(a),晶体内部氧空位调控(b)及材料肿瘤治疗-骨缺损修复双功能:近红外光照射下,黑色生物陶瓷材料具有显著的升温效果(c),从而通过光热功能显著杀死体内骨肿瘤并抑制其复发(d),与传统白色生物陶瓷(WCS)相比,黑色生物活性陶瓷在体内兔子股骨缺损修复中表现出更佳的诱导骨组织再生的活性(e)。
2. 软组织肿瘤治疗-组织缺损修复多功能支架
课题组进一步将多功能生物材料的应用从硬组织骨肿瘤治疗拓展到软组织肿瘤性皮肤创伤治疗以及乳腺癌等治疗,拓宽了多功能生物陶瓷材料的应用范围。
受中国芝麻棒设计策略的启发,课题组采用自旋涂布技术将CaCuSi4O10纳米颗粒涂覆在电纺纤维表面制备了一种芝麻棒状电纺纳米纤维支架,芝麻棒状支架能有效通过光热疗法,抑制早期体内肿瘤生长。同时,通过局部释放具有生物活性的Cu2+和SiO44-离子刺激体内血管生成和再上皮化促进慢性伤口愈合(如图24所示,Biomaterials 2019, 194: 25-35)。
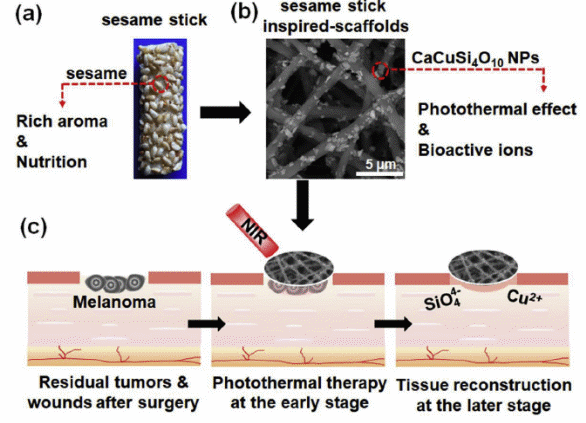
图24 .仿生芝麻棒纳米纤维支架用于皮肤肿瘤治疗和皮肤组织重建
课题组基于锰(Mn)离子在促角质细胞迁移、光热抗肿瘤、饥饿疗法抗肿瘤的研究基础上,将Mn离子与硅酸盐相结合,利用水热法制备硅酸锰空心纳米球(MSHNPs),将其装载葡萄糖氧化酶(GOx)后,将载酶的MSHNPs掺入到海藻酸钠水凝胶中,得到硅酸锰复合水凝胶(G/MS-5SA)。体外、体内抗肿瘤结果显示光热和饥饿疗法的协同作用导致最高的肿瘤细胞死亡率。在体内创面修复的实验中,与单纯的海藻酸钠水凝胶相比,MSHNPs的引入能明显促进新生皮肤伤口处的上皮化过程。饥饿治疗/光热协同抗肿瘤有利于增加黑色素瘤治疗疗效,多功能硅基生物活性材料能为临床肿瘤治疗和术后伤口管理提供新的策略与研究方向(如图25所示,Bioactive Materials, 2021, 6: 4558–4567)。
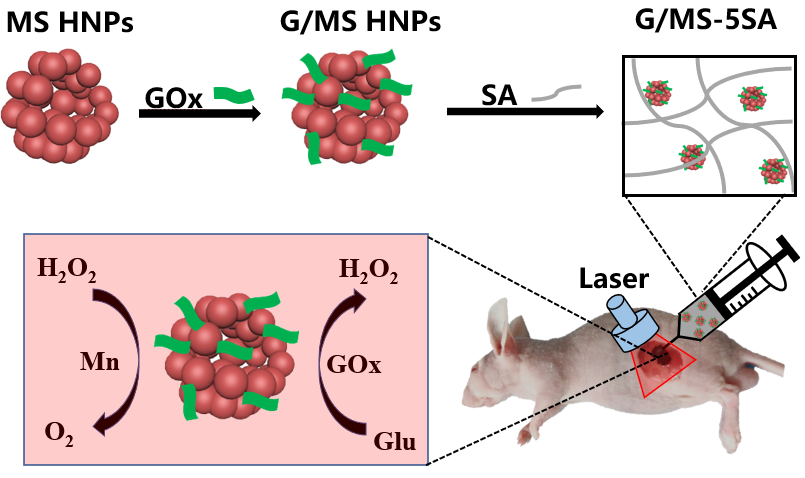
图25.硅酸锰空心纳米球复合水凝胶用于光热/饥饿治疗黑色素瘤及皮肤创面修复示意图
乳腺癌已经成为女性最常见的癌症。亟需开发一种兼具肿瘤治疗与诱导脂肪组织再生的材料用于治疗乳腺癌手术切除引起的组织缺损。课题组利用3D打印技术制备出兼具肿瘤治疗及脂肪再生的Fe3O4-CS-GelMA复合水凝胶支架。研究发现复合水凝胶支架具有良好的磁热性能,能够有效杀死4T1乳腺癌细胞。硬硅钙石释放活性离子SiO44-可促进成脂相关基因(PPARγ、Leptin、Adiponectin、FABP4)的表达,并通过PI3K-AKT信号通路有效促ADSCs的相关基因和蛋白。原位乳腺癌模型动物实验结果可以发现Fe3O4-CS-GelMA支架在交变磁场下能够杀死乳腺癌细胞,且两周后肿瘤没有复发。裸鼠体内实验表明添加ADSCs的CS-GelMA支架能明显促进体内脂肪的形成。本研究为乳腺癌手术切除后乳腺肿瘤的治疗提供了一个有希望的策略(如图26所示,Nano Letters 2023, 23(15): 7157-7165)。
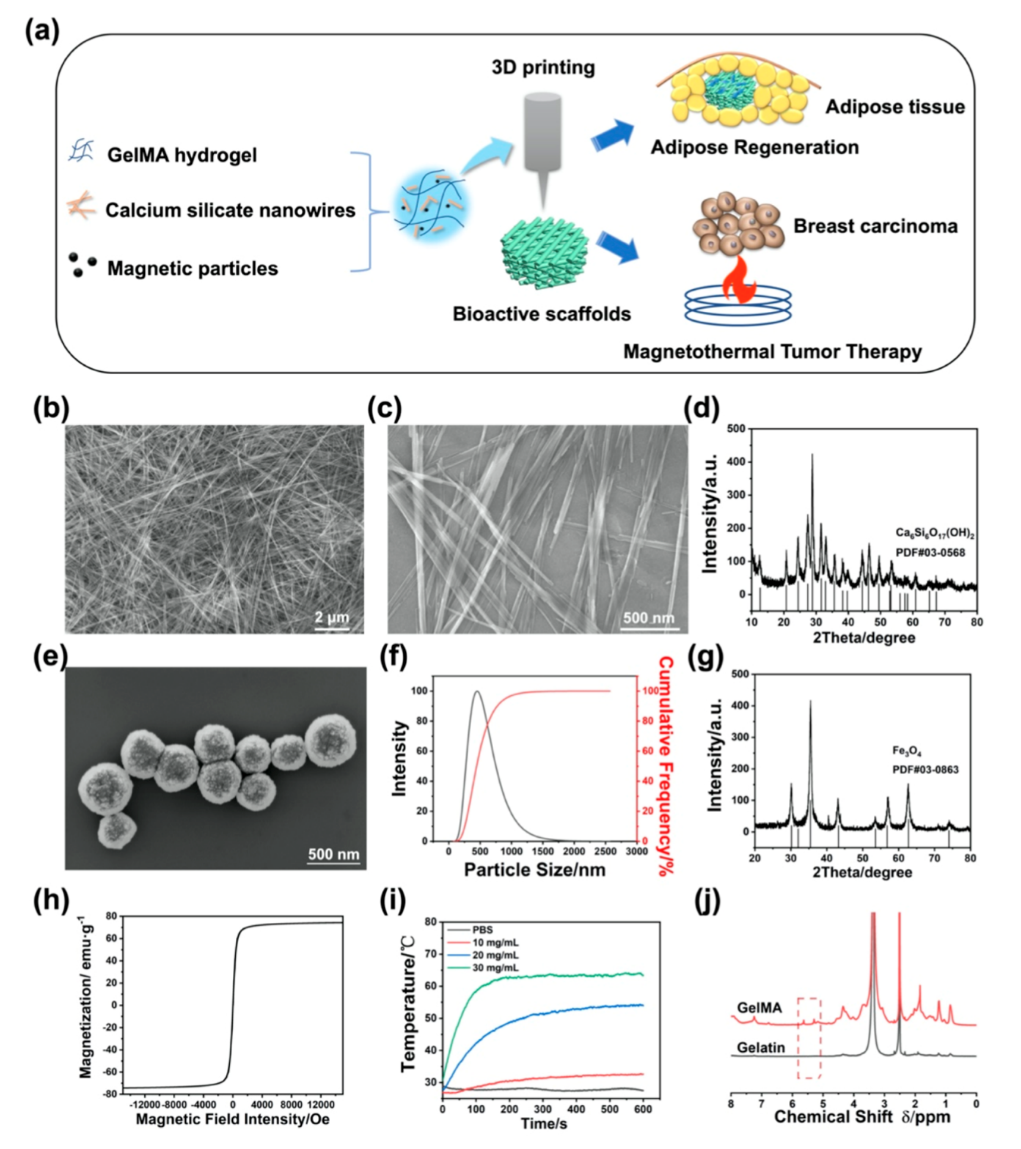
图26. 3D打印生物活性Fe3O4-CS-GelMA复合支架的制作过程示意图,及其在乳腺癌手术切除后脂肪组织再生和乳腺肿瘤磁热治疗中的应用。


 沪公网安备 31010502006565号
沪公网安备 31010502006565号